Билярд / Билярд / Гети изображения
Основни продукти за вкъщи
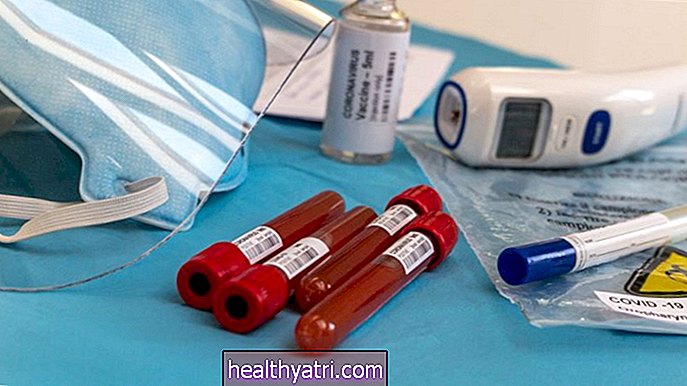
- FDA даде разрешение за спешна употреба на ваксината COVID-19, разработена от Pfizer и BioNTech.
- Новината идва ден след като консултативният комитет на FDA препоръча агенцията да разреши ваксината
- Данните, прегледани от комисията, установиха, че ваксината е 95% ефективна.
- Разпределението на ваксините може да стане в рамките на 24 часа след разрешението.
В петък вечерта Администрацията по храните и лекарствата (FDA) даде разрешение за спешна употреба на първата си ваксина COVID-19. Ваксината, разработена от Pfizer Inc. и немската компания BioNTech, ще започне разпространението си скоро.
Новината е след дългоочакваното публично изслушване в четвъртък, по време на което консултативен комитет към FDA гласува 17-4 в подкрепа на разрешението за ваксината Pfizer, с един въздържал се.
Pfizer представи данни от клинични проучвания, включващи 43 000 възрастни участници.По-рано тази седмица FDA сподели част от тези данни, включително факта, че 95% от хората в клиничното изпитване, получили ваксината, не са продължили да развиват COVID -19. Нежеланите реакции са незначителни, включително студени тръпки, лека болка и зачервяване на мястото на инжектиране.
Разрешението за спешна употреба (EUA) се прилага за хора на възраст 16 и повече години. Pfizer също така провежда клинични изпитвания за безопасността и ефикасността на ваксината при деца на възраст до 12 години и се очаква да добави опити и за по-малки деца.
Все още са необходими данни за безопасност и ефикасност от повече популации
Консултативният комитет на FDA, наречен Консултативен комитет за ваксини и свързани биологични продукти (VRBPAC), препоръчва на Pfizer да предприеме допълнителни мерки, за да се увери, че ваксината е безопасна и ефективна за повече популации. Панелът съветва повече цветни хора да бъдат добавени към текущи клинични изпитвания. Цветните хора са по-склонни от белите хора да заразят COVID-19 и да умрат от вируса.
Панелът обсъди и два докладвани случая на алергични реакции при хора, получили ваксина в Обединеното кралство тази седмица, където тя вече е одобрена. Пол Офит, д-р, директор на Центъра за обучение по ваксини в Детската болница във Филаделфия, попита водещите на Pfizer за алергичните реакции, загрижени, че хората с тежки алергии могат да изберат да не вземат ваксината. Offit препоръчва да се провеждат проучвания и за ваксината при хора с често срещани алергии.
Обединеното кралство препоръчва хората с анамнеза за анафилаксия към лекарство или храна да не получават ваксината. САЩ могат да добавят подобно предупреждение в тандем с разрешение. Служителите на FDA на срещата казаха на панела, че вече работят по писмена документация за потребителите относно безопасността и ефективността на ваксината.
Какво означава това за вас
Въз основа на препоръка от консултативен комитет за разрешаване на ваксината COVID-19 на Pfizer, Администрацията по храните и лекарствата може да одобри употребата й до дни. Разпространението може да започне много скоро след това.Очаква се първите дози от ваксината да бъдат приложени на здравни работници и обитатели на домове за възрастни хора.
След решението на VRBPAC, комисарят на FDA, Стивън М. Хан, д-р излезе с изявление:
„Обикновено процесът на преглед на ваксините, изследвани при десетки хиляди хора, отнема месеци. Въпреки че процесът беше ускорен във връзка с прегледа на този EUA, експертният екип на FDA прегледа хиляди страници техническа информация [включително] данни от клинични изпитвания, неклинични данни за развитието на ваксината в лабораторията, и производствени данни за това как се прави ваксината. "
Хан, който вероятно се стреми да разсее страховете сред потребителите, добави: „По това време на голяма спешност служителите на FDA чувстват отговорността да преминат възможно най-бързо през процеса на преглед. Те обаче знаят, че трябва да изпълняват мандата си за защита на общественото здраве и да гарантират, че всяка разрешена ваксина отговаря на нашите строги стандарти за безопасност и ефективност, които американският народ очаква. “
Избраният президент Джо Байдън също излезе с изявление след гласуването в комисията, в което се казва, „целостта на науката ни доведе до този момент“.
FDA казва, че разпространението на ваксини може да стане в рамките на 24 часа след разрешението.
Консултативният комитет на FDA ще прегледа втората ваксина срещу COVID-19, направена от Moderna, в четвъртък, 17 декември.