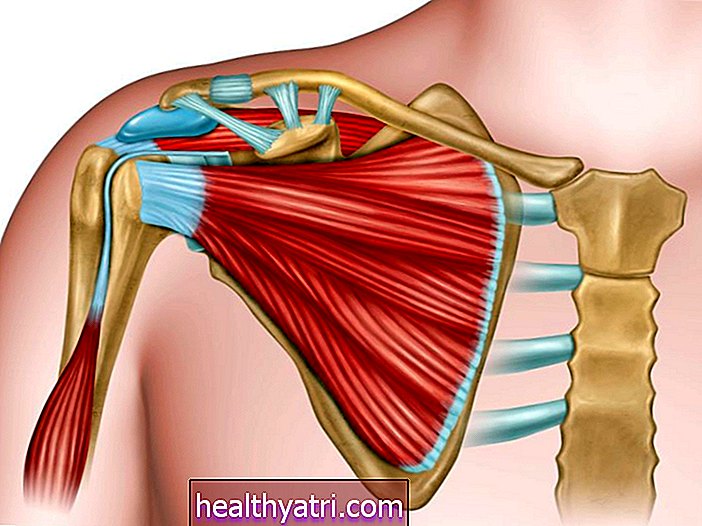
digicomphoto / Гети изображения
Основни продукти за вкъщи
- Veklury (ремдезивир) е първото одобрено от FDA лечение за хора с COVID-19.
- Одобрението е само за лечение при хоспитализирани пациенти над 88 паунда.
- Преди това лекарството имаше разрешение за спешна употреба от FDA.
В четвъртък Администрацията по храните и лекарствата (FDA) одобри Veklury (ремдезивир) за лечение на COVID-19 при хоспитализирани пациенти на 12 и повече години. Това е първото официално одобрено от FDA лекарство за COVID-19.
Преди това FDA е издала разрешение за спешна употреба (EUA) за ремдезивир, но не е пълно одобрение. Първият EUA, издаден на 1 май, казва, че ремдезивир може да се използва при хоспитализирани пациенти с тежък COVID-19. EUA беше преиздаден на 28 август, разширявайки употребата на хоспитализирани възрастни и деца с потвърдени или подозирани случаи COVID-19, независимо от тежестта на заболяването.
Въпреки че лекарството вече е одобрено, одобрението не се разпростира върху всички групи. Пациентите трябва да тежат най-малко 40 килограма (кг) - около 88 паунда - за да получат ремдезивир. В опит да продължи да предлага лекарството на педиатрични пациенти, обхванати от първия EUA, когато е необходимо, FDA преиздадедругEUA за използване на редезивър в:
- Хоспитализирани педиатрични пациенти с тегло от 3,5 kg до по-малко от 40 kg
- Хоспитализирани педиатрични пациенти на възраст под 12 години с тегло най-малко 3,5 kg
„FDA се ангажира да ускори разработването и предлагането на лечения с COVID-19 по време на тази безпрецедентна извънредна ситуация в областта на общественото здраве“, заяви в изявление комисарят на FDA Стивън М. Хан. „Днешното одобрение се подкрепя от данни от множество клинични изпитвания, които агенцията е направила стриктно оценка и представлява важен научен крайъгълен камък в пандемията на COVID-19. Като част от Програмата за ускоряване на лечението на коронавируса на FDA, агенцията ще продължи да помага за преместването на нови медицински продукти на пациентите възможно най-скоро, като в същото време определя дали те са ефективни и дали ползите им надвишават рисковете. “
Какво представлява Remdesivir?
Ремдезивир е антивирусно лекарство с директно действие, което инхибира синтеза на вирусна рибонуклеинова киселина (РНК) .Коронавирусите, включително SARS-CoV-2, са семейство от едноверижен РНК геном. Доказано е, че ремдезивир спира възпроизвеждането на тези вируси.
Ремдезивир и COVID-19
Ремдезивир за пръв път заглави заглавия през пролетта, когато изследователите от Тексас определиха интравенозното лекарство като „най-обещаващата терапия“ за COVID-19 въпреки ограничените клинични данни.
Когато се появи SARS-CoV-2, изследователите видяха обещаващи резултати след тестване на ремдезивир върху вируса в лаборатория и скоро след това започнаха клинични изпитвания, обяснява д-р Матю Д. Хол, който работи в Националния център за развитие на транслационните науки в Националния Институти по здравеопазване. Той помогна за създаването на портала OpenData на COVID-19 за споделяне на данни за пренасочване на лекарства и експерименти, свързани с COVID-19, за всички одобрени лекарства.
„Повечето одобрени лекарства отнемат средно 15 години и няколко милиарда долара, за да се развият средно“, казва Хол пред Verywell. „Но нямахме 15 години; нямахме дори 15 седмици. "
Хол казва, че той и екипът му са били натоварени да оценят съществуващите ресурси.
„Трябваше да се огледаме за нещата, които вече бяха на разположение за нас, или бяха одобрени за лечение на други заболявания, или бяха разработени за лечение на други заболявания“, казва той. "Все още може да не са одобрени, но дано са били при хора и знаем, че са в безопасност. Имаме късмета да имаме много антивирусни лекарства. От тези лекарства, които са одобрени, или кандидати за наркотици, ремдезивир изглежда са били най-активни, поради което може да се премине към клинични изпитвания много бързо. "
Матю Д. Хол, д-р
Повечето одобрени лекарства отнемат средно 15 години и няколко милиарда долара, за да се развият средно. Но нямахме 15 години; нямахме дори 15 седмици.
- Матю Д. Хол, д-рFDA първоначално предостави EUA на 1 май, за да позволи на хоспитализирани възрастни пациенти с тежък COVID-19 да бъдат лекувани с ремдезивир. Лице с тежък COVID-19 беше определено като:
- Пациент с насищане с кислород по-малко или равно на 94%
- Пациент, нуждаещ се от допълнителен кислород
- Пациент, който се нуждае от механична вентилация
- Пациент, който се нуждае от екстракорпорална мембранна оксигенация
Разширената EUA помогна да се направи лекарството достъпно за пациенти на по-ранни етапи или с по-леки случаи на заболяването, а одобрението трябва само да увеличи неговата наличност. Хол казва, че пациентите не трябва да бъдат регистрирани като част от клинична пътека, за да получат лечение, увеличавайки достъпа на хора, живеещи в селските общности, които не живеят в близост до изследователски центрове.
„Мисля, че всички сме съгласни, че би било добре хората, които са малко зле вкъщи, да вземат антивирусно средство, за да изкоренят вируса от телата си по-рано, за да се уверят, че по-късно не се разболяват“, казва Хол. „В момента трябва да изчакате, докато не се разболеете, за да лежите в болница, за да получите ремдезивир. Би било чудесно да се уверите, че тези хора никога не са достатъчно болни, за да отидат в болницата, като им дадете антивирусно средство по-рано като Тамифлу за грип, (където) отидете на лекар, вземете хапчето и това ще съкрати времето, което болен съм за. ”
Развитие на Remdesivir
Ремдезивир първоначално е разработен като част от сътрудничеството между Gilead Sciences, Центровете за контрол и превенция на заболяванията в САЩ и Института по инфекциозни болести на Американската армия. Той е изследван като потенциално терапевтично средство по време на епидемията от западноафриканския вирус Ебола и за два други коронавируса: тежък остър респираторен синдром (SARS) и респираторен синдром в Близкия изток (MERS).
Кой трябва да приема Remdesivir?
Оптималната популация пациенти на Remdesivir, дозирането и продължителността на лечението не са известни. В информационен лист за доставчиците на здравни услуги FDA предлага следните препоръки:
- За възрастни и педиатрични пациенти с тегло над 40 kg и повече, препоръчителната доза е 200 mg на 1 ден, последвана от следващи дози от 100 mg.
- За педиатрични пациенти с тегло между 3,5 kg и 40 kg препоръчителната доза е 5 mg / kg на 1-ви ден, последвана от последващи дози от 2,5 mg / kg.
- За пациенти, които не се нуждаят от инвазивна механична вентилация и / или екстракорпорална мембранна оксигенация, препоръчителната обща продължителност на лечението е 5 дни.
- За пациенти, които се нуждаят от инвазивна механична вентилация и / или екстракорпорална мембранна оксигенация, препоръчителната обща продължителност на лечението е 10 дни.
- Ако пациентът не демонстрира клинично подобрение, лечението може да бъде удължено до 5 допълнителни дни за обща продължителност на лечението до 10 дни.
Gilead Sciences работи за увеличаване на производството и разпространението на ремдезивир, който се счита за изследвано лекарство и понастоящем не е одобрен за каквито и да е показания.
Клинични изпитвания и предварителни констатации
Решението на FDA да одобри ремдезивир се основава на резултатите от няколко клинични проучвания и е срещнато със смесени мнения от медицинската общност.
„Какво мисля за дадено лекарство или кандидат за наркотици всъщност няма значение“, казва Хол. „Това, което наистина има значение, са данните от добре контролирано клинично изпитване. FDA нямаше да разшири обхвата на EUA, ако не смятаха, че ще има полза за повече пациенти. "
В проучване, публикувано на 29 април вThe Lancet,група лекари и изследователи проведоха рандомизирано, двойно-сляпо, плацебо-контролирано проучване на 237 възрастни пациенти с тежък COVID-19 в 10 болници в Хубей, Китай.Те откриха, че ремдезивир помага за ускоряване на възстановяването.
„Макар и да не са статистически значими, пациентите, получаващи ремдезивир, са имали числено по-бързо време до клинично подобрение, отколкото тези, получаващи плацебо сред пациенти със продължителност на симптомите 10 дни или по-малко“, пишат авторите.
Проучване, финансирано от правителството на САЩ, публикува предварителните си констатации на 22 май вNew England Journal of Medicineот рандомизирано, двойно-сляпо плацебо-контролирано проучване на 1063 пациенти с COVID-19. Изследователите установяват, че тези, на които е назначен 10-дневен курс на ремдезивир, имат по-кратко време за възстановяване в сравнение с плацебо - медиана от 11 срещу 15 дни.
„Тези предварителни открития подкрепят използването на ремдезивир за пациенти, които са хоспитализирани с COVID-19 и се нуждаят от допълнителна кислородна терапия“, пишат авторите. „Въпреки това, предвид високата смъртност въпреки употребата на ремдезивир, е ясно, че лечението само с антивирусно лекарство вероятно няма да бъде достатъчно.“
На 21 август,Вестник на Американската медицинска асоциацияпубликува рандомизирано проучване фаза 3 на 584 пациенти, хоспитализирани с умерена пневмония COVID-19. Производителят на Remdesivir Gilead Sciences спонсорира това проучване в 105 болници в САЩ, Европа и Азия. Пациентите са получавали 5-дневен или 10-дневен курс на ремдезивир или са получавали стандартни грижи. Изследователите не откриха разлика в резултатите сред 10-дневната група и малка значима разлика сред 5-дневната група.
И трите проучвания са изправени пред различни ограничения и имат важни дизайнерски разлики, така че не е честно да се създава сравнение между ябълки и ябълки. Това обаче повдига въпроси относно възпроизвеждането на откритията, отличителен белег на клиничните изследвания.
„В момента има три [рандомизирани контролни проучвания] на ремдезивир при хоспитализирани пациенти с различни резултати, повдигайки въпроса дали несъответствията са артефакти от избора на дизайн на изследването, включително популации пациенти, или дали лекарството е по-малко ефикасно от очакваното“, University of Изследователите от Питсбъргското училище по медицина пишат в статия, публикувана вВестник на Американската медицинска асоциацияна 21 август. „Следователно изглежда разумно да се извършат спешни допълнителни оценки на ремдезивир в широкомащабни рандомизирани контролни проучвания, предназначени за справяне с остатъчните несигурности и информиране за оптимална употреба.
Какво означава това за вас
Американската администрация по храните и лекарствата е издала първото си одобрение за лечение на COVID-19 на ремдезивир. Ако сте хоспитализирани с потвърден или подозиран случай на COVID-19, вашият доставчик на здравни грижи може да реши да предпише това лекарство.
Какво следва за Remdesivir?
Текат още клинични изпитвания, според уебсайта на Gilead Sciences. Компанията също е в първата фаза на разработване, за да формулира ремдезивир като инхалатор.
Хол казва, че глобалната общност се е справила с предизвикателството, но търсенето на лекарство за SARS-CoV-2 се е усложнило от факта, че няма терапевтични средства за човешки коронавируси. Неотдавнашните огнища на ТОРС и MERS се борят с мерки за обществено здраве, а не с терапевтични средства.
„С ремдезивир имаме голям късмет, че е съществувал“, казва Хол. "Имаме късмет, че е разработен за ебола. Имаме късмет, че той вече е на разположение за тестване при хора. Защото ако извадите ремдезивир от уравнението, не знам какво е следващото най-добро нещо. друго лекарство, одобрено за лечение на SARS-CoV-2 инфекция. "


















.jpg)