
CMB / Гети изображения
Основни продукти за вкъщи
- Няколко големи биофармацевтични компании обещаха да гарантират, че ваксината няма да бъде изпратена за одобрение от правителството, докато не бъде безопасна и ефективна.
- Обещанието пристига сред нарастващото недоверие към сроковете за разработване на ваксини.
- Декларацията не променя мерките за безопасност, които вече съществуват за разработване на ваксина срещу COVID-19.
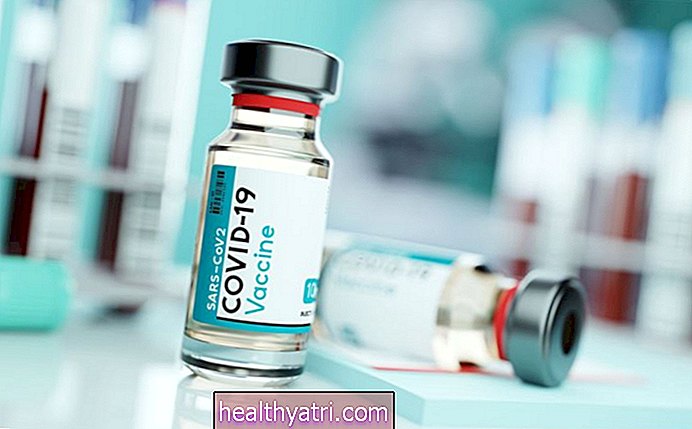
Девет големи биофармацевтични компании обещаха във вторник да търсят одобрение само за ваксини COVID-19, за които е доказано, че са безопасни и ефективни. Този ход идва на върха на нарастващите опасения, че настояването за бързо разработена ваксина COVID-19 е политически мотивирано.
Главните изпълнителни директори на AstraZeneca, BioNTech, GlaxoSmithKline, Johnson & Johnson, Merck, Moderna, Novavax, Pfizer и Sanofi подписаха обещанието. Конкуриращите компании включват трите водещи усилия за ваксина срещу COVID-19, които са напреднали в последния етап на клиничните изпитвания.
„Ние, долуподписаните биофармацевтични компании, искаме да изясним текущия си ангажимент за разработване и тестване на потенциални ваксини за COVID-19 в съответствие с високи етични стандарти и здрави научни принципи“, се казва в обещанието.
В тяхното изявление се казва, че безопасността и ефикасността на ваксините - включително ваксина срещу COVID-19 - се преглеждат и определят от регулаторните агенции по света, включително Администрацията по храните и лекарствата (FDA).
„FDA е установила ясни насоки за разработването на ваксини COVID-19 и ясни критерии за тяхното потенциално разрешаване или одобрение в САЩ“, се казва в обещанието. „Насоките и критериите на FDA се основават на научните и медицински принципи, необходими за ясното демонстрират безопасността и ефикасността на потенциалните ваксини срещу COVID-19. "
Обещанието продължава да обяснява изискванията на FDA за регулаторно одобрение:
- Научните доказателства трябва да идват от големи, висококачествени клинични изпитвания.
- Изпитанията трябва да бъдат заслепени от наблюдатели и рандомизирани.
- Трябва да има значителен брой участници, привлечени от различни популации.
Ваксини COVID-19: Бъдете в течение с наличните ваксини, кой може да ги получи и колко безопасни са.
Въз основа на указанията на FDA фармацевтичните компании казват, че ще направят следното:
- Винаги поставяйте безопасността и благосъстоянието на ваксинираните лица за основен приоритет.
- Продължавайте да се придържате към високите научни и етични стандарти по отношение на провеждането на клинични изпитвания и строгостта на производствените процеси.
- Представяйте за одобрение или разрешение за спешна употреба само след демонстриране на безопасност и ефикасност чрез клинично проучване Фаза 3, което е проектирано и проведено в съответствие с изискванията на експертни регулаторни органи като FDA.
- Работете за осигуряване на достатъчни доставки и гама от възможности за ваксина, включително тези, подходящи за глобално разпространение.
Какво означава това за вас
Въпреки че залогът звучи добре, той не променя никакви протоколи за безопасност около разработването на ваксина срещу COVID-19. По-скоро просто потвърждава ангажимента на биофармацевтичните компании към съществуващия им стандарт.
Причината за обещанието
Биофармацевтичните компании заявиха, че вярват, че този залог ще спомогне за гарантиране на общественото доверие към ваксините COVID-19, които понастоящем се подлагат на строги, научни процеси за оценка. Отговорът им дойде бързо, след като президентът Доналд Тръмп обеща да има готова ваксина преди президентските избори през ноември.
„Може да ви предстои много голяма изненада. Сигурен съм, че ще бъдете много щастливи. Но хората ще бъдат щастливи. Хората по света ще бъдат щастливи ”, каза президентът Доналд Тръмп пред репортери, предаде ABC News. „Ще имаме ваксина много скоро, може би дори преди много специална дата. Знаете за коя дата говоря. "
Но висши служители в областта на общественото здравеопазване заявиха, че това е малко вероятно. Д-р Монсеф Слауи, главен научен ръководител на операцията Warp Speed - усилията на администрацията на Тръмп за бързо проследяване на ваксината - каза пред NPR миналата седмица, че наличието на ваксина преди изборите е „изключително малко вероятно, но не и невъзможно“. Слауи също така каза, че има „много, много малък шанс“ клиничните изпитвания за ваксина да приключат преди края на октомври и че ще има разрешение за спешна употреба от FDA навреме.
Д-р Антъни Фаучи, директор на Националния институт по алергия и инфекциозни болести, наскоро каза пред репортери в Research! Национален форум за изследване на здравето на Америка 2020, че е малко вероятно да имаме окончателен отговор за ваксината до изборите в началото на ноември. Вместо това, каза той, ваксина вероятно ще бъде готова до „края на годината“.
Реакциите на обществеността са смесени
Ново проучване на безпартийната фондация на семейство Кайзер установи, че 62% от американските респонденти се притесняват, че политическият натиск от администрацията на Тръмп ще накара FDA да бърза да одобри коронавирусна ваксина, без да се увери, че е безопасна и ефективна.
Ако ваксината срещу COVID-19 бъде одобрена от FDA преди изборите и бъде предоставена и безплатна за всички, които я искат, само четирима от всеки десет възрастни казват, че биха искали да се ваксинират, според анкетата.
Много хора изразиха в социалните медии, че обещанието изглежда ненужно. „Това необходимо ли е по някаква причина? Очевидна отговорност, която фармацевтичните компании трябва да спазват, без да се налага да го казват? " един човек написа в Twitter. „Това е нещо без умове. Нито една компания не иска да бъде тази компания, която пуска ваксина, която създава повече проблеми, отколкото решава “, каза друг.
„Странно е, че изчакването на доказателства за безопасност се представя като ново или извън разумни очаквания. Защо заблуждавате обществеността? “ един написа. "Еха. Това е добре, но и тъжно “, беше отговорът на друг туитър.
Къде стоят сега опитите за ваксини
В момента има най-малко 93 предклинични ваксини, подложени на активно разследване върху животни, и 38 ваксини, които са в проучвания при хора, според проследяването на коронавирусната ваксина на The New York Times.
Девет от тези ваксини са във фаза 3 от клиничните изпитвания, които включват мащабни тестове върху хора. Три от ваксините са одобрени за ранна или ограничена употреба, включително две от китайски компании и една от изследователски институт в Русия.
Изпитванията на AstraZeneca за фаза 3 срещу COVID-19 наскоро бяха спрени, след като жена, участваща в проучването, разви неврологични симптоми, съответстващи на рядко, но сериозно гръбначно-възпалително разстройство, наречено напречен миелит, каза говорител на компанията пред ABC News. По-рано AstraZeneca заяви, че е решила да „направи пауза“ на изпитанието си, за да „позволи преглед на данните за безопасността“. По това време компанията предостави малко подробности, освен да каже, че участник е имал „необяснима болест“. Няма информация кога ще бъде възобновено изпитанието на ваксината.
Фармацевтичният залог завърши с последния призив за обществено доверие: „Вярваме, че този залог ще помогне да се гарантира общественото доверие в строгия научен и регулаторен процес, чрез който се оценяват ваксините COVID-19 и в крайна сметка могат да бъдат одобрени.“
Как точно действат ваксините?








.jpg)







-for-arthritis.jpg)


-for-crohns-disease.jpg)
