
Sasiistock / Getty Images
Основни продукти за вкъщи
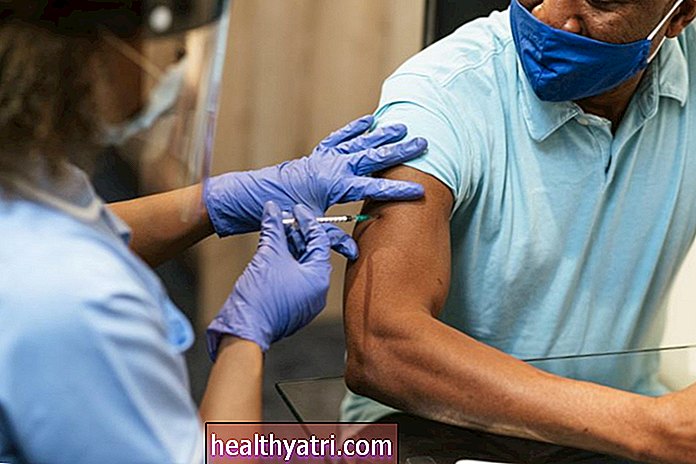
- Pfizer получи одобрение от FDA да започне да тества своята коронавирусна ваксина при деца на 12 и повече години.
- Експертите казват, че включването на деца в клинични изпитвания е от решаващо значение за цялостното разработване на ваксина, която ще предпази както децата, така и възрастните от COVID-19.
- Според уебсайта си Pfizer вече е включил повече от 39 000 доброволци в своето проучване. Повече от 34 000 от тези доброволци вече са получили втора ваксинация.
Американската фармацевтична компания Pfizer обяви през октомври, че е получила разрешение от Американската администрация по храните и лекарствата (FDA) да започне да записва деца на възраст до 12 години в своите проучвания за ваксинация срещу коронавирус.
„По този начин ще можем да разберем по-добре потенциалната безопасност и ефикасност на ваксината при лица от повече възрасти и произход“, се казва в актуализираното изявление на компанията.
Това ще бъде първото изпитание за ваксина срещу COVID-19 в САЩ, което включва деца. Към октомври Pfizer е една от четирите американски компании, които имат ваксини във фаза 3 клинични изпитвания.
Pfizer вече беше разширил фаза 3 от своето проучване, за да включи деца на 16 и повече години, както и хора с хроничен, стабилен човешки имунодефицитен вирус (ХИВ), хепатит С и хепатит В.
Защо да тествате ваксина COVID-19 при деца?
Преди Pfizer да получи одобрение да започне тестване при деца, експертите публикуваха доклад в списаниетоКлинични инфекциозни болестикато се посочва важността на такова тестване.
„Прякото въздействие на COVID-19 върху децата е по-голямо от това, наблюдавано за редица други патогени, за които сега имаме ефективни педиатрични ваксини“, се отбелязва в доклада. „Освен това ролята на децата в предаването на SARS-CoV-2 очевидно е недооценена. Внимателно проведените клинични изпитвания във фаза 2 могат да отговорят адекватно на потенциалните опасения за безопасността на ваксината срещу COVID-19.
Сузани Фам, д-р
Не можем да преодолеем разпространението на този вирус, ако не ваксинираме децата си.
- Сюзан Фам, д-рШарън Нахман, д-р, ръководител на отдела за детски инфекциозни болести в Детска болница Stony Brook в Ню Йорк, се съгласява с доклада, като казва на Verywell, че „педиатрите са много заинтересовани да видят подробностите на проучването и как ще действа ваксината при децата . "
Според Nachman тестването на ваксината при деца има специфични ползи. Изследователите ще могат да оценят краткосрочния и дългосрочния имунен отговор, който включва изчисляване дали дозата ваксина, използвана при възрастни, е необходима за деца или ако те биха имали подобен имунен отговор на по-ниска доза.
Nachman казва, че е важно също така да се отбележи, че тъй като коронавирусът при възрастни може да бъде предшестван от излагането им на асимптоматична инфекция при деца, създаването на ваксина за лечение на цялото семейство може да „направи дълъг път за намаляване на предаването у дома и в общността“.
Д-р Сузани Фам, асоцииран главен медицински директор в болница Weiss Memorial в Чикаго, казва на Verywell, че колкото по-скоро децата могат да бъдат ваксинирани, толкова по-скоро скоростта на предаване ще намалее.
„Чрез ефективното ваксиниране на децата рискът от предаване на вируса в общността ще намалее, особено при онези високорискови хора, които са по-податливи на тежки или критични заболявания“, казва Фам пред Verywell. „Това ще позволи на училищата да започнат да се отварят отново и дейностите, жизненоважни за развитието на нашите деца, да се възобновят по контролиран начин. Не можем да преодолеем разпространението на този вирус, ако не ваксинираме децата си. Трябва да имаме достатъчно стаден имунитет в обществото, за да можем да предотвратим разпространението “.
Ваксини COVID-19: Бъдете в течение с наличните ваксини, кой може да ги получи и колко безопасни са.
Как започват изпитанията с ваксини?
Фам обяснява, че за да бъде тествана ваксина - за възрастни или деца - компанията трябва първо да подаде заявление за изследване на нови лекарства (IND) до FDA.
Заявлението ще опише ваксината, как се произвежда и какви тестове за контрол на качеството трябва да се използват. Приложението включва и данни от тестове върху животни, които показват, че ваксината е безопасна за първоначално тестване при хора.
Както обяснява FDA, процесът на кандидатстване има няколко стъпки:
По време на ранното предклинично развитие на ново лекарство, основната цел на спонсора е да определи дали продуктът е разумно безопасен за първоначална употреба при хора и дали съединението проявява фармакологична активност, която оправдава търговското развитие.
Когато даден продукт бъде определен като жизнеспособен кандидат за по-нататъшно развитие, спонсорът след това се фокусира върху събирането на данните и информацията, необходими, за да се установи, че продуктът няма да изложи хората на неразумни рискове, когато се използва в ограничени клинични проучвания в ранен етап.
След това ваксината ще бъде подложена на изпитвания от фаза 1, за които Фам обяснява, че са „проучвания за безопасност и имуногенност, направени при малък брой хора, които се наблюдават внимателно“.
„Фаза 2 се състои от проучвания за определяне на дозата и се разширява до по-голям брой (стотици) хора“, казва Фам. „Тогава изпитанията във Фаза 3 се стремят да включат хиляди хора, за да документират ефективността и да продължат да разглеждат данните за безопасността.“
Според уебсайта си Pfizer е включил повече от 39 000 доброволци в своето проучване. Повече от 34 000 от тях са получили втора доза от ваксината.
Какво означава това за вас
Клинично изпитване фаза 3, което включва тестване на ваксина COVID-19 при деца, е знак за напредък. Ваксината обаче не може да се бърза. Финализирането на резултатите отнема време, за да се защити безопасността на участниците в изпитването, както и на възрастни и деца, които в крайна сметка ще получат готовата версия на ваксината.






-in-sleep.jpg)













.jpg)

.jpg)
