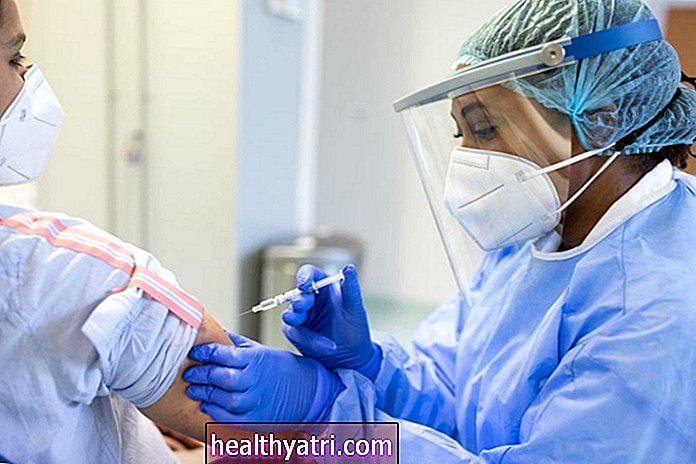
Елън Линднер / Много добре
Основни продукти за вкъщи
- Две базирани на иРНК ваксини са получили бързо обозначение от FDA.
- Докато бързият статус ще ускори разработването и потенциалния процес на одобрение, Pfizer и BioNTech са отказали всякакво федерално финансиране за ваксина срещу COVID-19.
- Ако клиничните изпитвания са успешни, началните дози могат да бъдат готови до края на годината.
Pfizer и BioNTech обявиха в понеделник, че двама от кандидатите им за коронавирусна ваксина са получили обозначение „ускорено“ от Администрацията по храните и лекарствата (FDA).
Pfizer - американска фармацевтична компания - и BioNTech - немска биотехнологична фирма - се обединиха още през март, за да преследват ваксини срещу SARS-CoV-2, вирусът, който причинява COVID-19. По-конкретно, те създават ваксини с различни комбинации от messenger RNA (mRNA), метод, по който двойката работи заедно за противогрипни ваксини от 2018 г.
Ваксини COVID-19: Бъдете в течение с наличните ваксини, кой може да ги получи и колко безопасни са.
Какво означава Fast Track?
Бързият процес на FDA улеснява ускореното разработване и преразглеждане на лекарства - или ваксини - предназначени „за лечение на сериозни заболявания и„ запълване на неудовлетворени медицински нужди “.
Няколко лекарства получават бързо обозначение всяка година. Към юни 20 лекарства бяха одобрени за ускоряване през 2020 г., в процес на разработване за условия, вариращи от метастатичен тройно отрицателен рак на гърдата до заболяване на щитовидната жлеза.
Лекарствените компании трябва да бъдат тези, които искат бързо определяне. Ако бъде одобрена, фармацевтичната компания може да очаква по-чести срещи, комуникация и подкрепа от FDA, както и право на ускорено одобрение и преглед на приоритетите.
Накрая говорител на FDA заяви пред Verywell, че на организацията е забранено да разкрива каквато и да е информация, съдържаща се в разследваното ново приложение на наркотици, така че има малко обществена информация за това защо са избрани именно тези кандидати. В съобщение за пресата, публикувано от Pfizer и BioNTech, се казва, че бързото обозначаване е последвано от "предварителни данни от проучвания фаза 1/2, които в момента продължават в Съединените щати и Германия, както и проучвания за имуногенност на животни."
Бързият път ще помогне на Pfizer и BioNTech да постигнат целта си да произведат до 100 милиона дози ваксини до края на 2020 г. в очакване на резултатите от текущите проучвания и одобрението на регулаторите. След това те потенциално ще произведат над 1,2 милиарда дози до края на 2021 година.
Ами други ваксини, получаващи финансиране от САЩ?
Pfizer и BioNTech по-специално не са в списъка на кандидатите за ваксини, получаващи финансиране от правителството на САЩ, който включва имена като AstraZeneca, Moderna и Johnson & Johnson. 19 инициатива за ваксини, председателят и главен изпълнителен директор на Pfizer Алберт Бурла казва, че са отказали федералното финансиране, за да се движат по-бързо.
„Когато взимате пари, хората, които ги дават, искат да знаят как сте ги похарчили и какво точно правите“, каза Бурла, споредPharma Intelligenceотразяване на виртуалния брифинг на института Milken през юни. „Скоростта беше от съществено значение в момента. Исках да се уверя, че ние даваме на нашите хора автономия да се движат бързо и да бягат и да могат да произвеждат ваксина. "
Как ще работят тези ваксини?
И двамата кандидати за ваксина, наричани BNT162b1 и BNT162b2, използват платформа за ваксини, зависима от mRNA, молекула, която помага на ДНК да произвежда протеин.
На теория, въвеждането на неинфекциозна вирусна иРНК ще подтикне тялото да създаде протеинови протеини, които покриват вируса SARS-CoV-2. Сами по себе си тези скокове са безвредни, но все пак ще предизвикат имунния отговор необходимо за създаване на антитела, които предпазват от ТОРС-CoV-2.
През последните години иРНК ваксините се доказаха по-безопасни, по-мощни и по-ефективни за производство от други видове ваксини, което прави технологията добър вариант за предвидените милиарди дози.
Pfizer и BioNTech планират да преминат към изпитания Фаза 2b / 3 възможно най-късно този месец с до 30 000 субекта.
Какво означава това за вас
Бързият път означава, че ако една или и двете ваксини се окажат безопасни и ефективни, процесът на одобрение от FDA ще се движи по-бързо. Това означава, че достъпността на ваксините за широката общественост може да се случи и по-бързо.